N88-BASICで滴定曲線 (5回目)
2021/11/5(金)
N88-BASICで滴定曲線 (5回目)
3価の酸と1価の強塩基の滴定曲線
(弱塩基だと式が複雑になりすぎたので
強塩基のみで式を作りました)
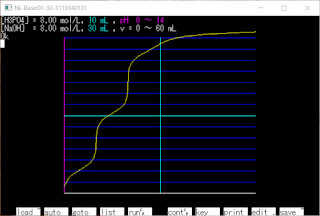
[H3PO4aqをNaOHaqで滴定]
水溶液(H2O)中に
[H3A],[H2A-],[HA2-],[H+],[A3-],[B+],[OH-]
が存在する
Ca = [A3-] + [H3A] + [H2A-] + [HA2-] … 酸の濃度
Cb = [B+] … 強塩基の濃度
Kw = [H+][OH-] … 水のイオン積
Ka1 = [H2A-][H+]/[H3A] … 酸の電離定数(第1)
Ka2 = [HA2-][H+]/[H2A-] … 酸の電離定数(第2)
Ka3 = [A3-][H+]/[HA2-] … 酸の電離定数(第3)
[B+] + [H+] = 3[A3-] + 2[HA2-] + [H2A-] + [OH-]
… 電気的中性(電荷の合計を比較している)
これを連立させる
(適当に求めたので煩雑かもしれません)
⇒ [B+] = Cb
Ka3 = [A3-][H+]/[HA2-] ⇒ [HA2-] = [A3-][H+]/Ka3
Ka2 = [HA2-][H+]/[H2A-] ⇒ [H2A-] = [HA2-][H+]/Ka2
= [A3-][H+]2/(Ka2Ka3)
Ka = Ka1Ka2Ka3 = [A3--][H+]3/[H3A]
= [A3--][H+]3/(Ca - [A3-] - [HA2-] - [H2A-])
⇒ [A3-][H+]3 - Ka(Ca - [A3-] - [HA2-] - [H2A-]) = 0
⇒ [A3-][H+]3 - Ka{Ca - [A3-] - [A3-][H+]/Ka3
- [A3-][H+]2/(Ka2Ka3)} = 0
⇒ [A3-]Ka2Ka3[H+]3 - Ka(CaKa2Ka3 - [A3-]Ka2Ka3
- [A3-][H+]Ka2 - [A3-][H+]2) = 0
⇒ [A3-] = KaKa2Ka3Ca/(Ka2Ka3[H+]3 + Ka[H+]2
+ KaKa2[H+] + KaKa2Ka3) = 0
3[A3-] + 2[HA2-] + [H2A-] + [OH-] - [B+] - [H+] = 0
3[A3-] + 2([A3-][H+]/Ka3) + [A3-][H+]2/(Ka2Ka3)
+ Kw/[H+] - Cb - [H+] = 0
[A3-]{3 + 2[H+]/Ka3 + [H+]2/(Ka2Ka3)}
+ Kw/[H+] - [H+] - Cb = 0
[A3-]{3[H+] + 2[H+]2/Ka3 + [H+]3/(Ka2Ka3)}
+ Kw - [H+]2 - Cb[H+] = 0
{3[H+] + 2[H+]2/Ka3 + [H+]3/(Ka2Ka3)}
KaKa2Ka3Ca/(Ka2Ka3[H+]3 + Ka[H+]2
+ KaKa2[H+] + KaKa2Ka3)
- [H+]2 - Cb[H+] + Kw = 0
3KaKa2Ka3Ca[H+] + 2KaKa2Ca[H+]2 + KaCa[H+]3
+ (Kw - [H+]2 - Cb[H+])(Ka2Ka3[H+]3 + Ka[H+]2
+ KaKa2[H+] + KaKa2Ka3) = 0
3KaCa[H+] + 2Ka1Ka2Ca[H+]2 + Ka1Ca[H+]3
+ (Kw - [H+]2 - Cb[H+])([H+]3 + Ka1[H+]2
+ Ka1Ka2[H+] + Ka) = 0
3KaCa[H+] + 2Ka1Ka2Ca[H+]2 + Ka1Ca[H+]3
+ Kw[H+]3 + KwKa1[H+]2 + KwKa1Ka2[H+] + KwKa
- [H+]5 - Ka1[H+]4 - Ka1Ka2[H+]3 - Ka[H+]2
- Cb[H+]4 - Ka1Cb[H+]3 - Ka1Ka2Cb[H+]2 - KaCb[H+]
= 0
[H+]5 + (Ka1 + Cb)[H+]4
+ (Ka1Ka2 + Ka1Cb - Ka1Ca - Kw)[H+]3
+ (Ka1Ka2Cb + Ka - 2Ka1Ka2Ca - KwKa1)[H+]2
+ (KaCb - 3KaCa - KwKa1Ka2)[H+] - KwKa = 0
[H+]5 + (Ka1 + Cb)[H+]4
+ {Ka1(Ka2 + Cb - Ca) - Kw}[H+]3
+ Ka1{Ka2(Ka3 + Cb - 2Ca) - Kw}[H+]2
+ Ka1Ka2{Ka3(Cb - 3Ca) - Kw}[H+]
- KwKa1Ka2Ka3 = 0
Ma, Mbを酸塩基それぞれのモル濃度、
Vaを酸の体積、Vbを塩基の滴定量とし
V = Va + Vb
Ca = MaVa/V
Cb = MbVb/V
で、滴定するたびに現在のモル濃度
Ca, Cbを計算し
上記、5次方程式をNewton法で解いて
滴定曲線(滴定量-pHのグラフ)を
描画しています
プログラム中で使用している数値は
適当に調べて書いていますので
正しいかどうかは自己責任で確かめて
下さい
Newton法は以下で説明しています
https://ulprojectmail.blogspot.com/2021/10/n88-basic-1.html
N88-BASICで天体の軌道(1回目)
NL-BASICとblg~.zip(neut005.bas)は
このブログ(以下のリンク)から
ダウンロードできます
https://ulprojectmail.blogspot.com
Readme.txtを読んで遊んで下さい